Module 1.4. Prematuren/neonaten
Uitgangsvraag
Welk huiddesinfectiemiddel is bij prematuren en neonaten effectief in het voorkómen van zorggerelateerde infecties en op welke wijze kan dit middel veilig gebruikt worden voorafgaand aan een ingreep?
Aanbevelingen
- Desinfecteer de huid van prematuren en neonaten voor een ingreep met 0,5-2% chloorhexidine in 70% alcohol.
Overwegingen
Voor- en nadelen van de interventie en de kwaliteit van het bewijs
Voor deze module is een systematische literatuuranalyse uitgevoerd naar welk huiddesinfectans effectief en veilig is in gebruik bij neonaten. Uit de literatuurselectie kwam een Cochrane review protocol van Muhd Helmi (2021) naar voren, waarvan in mei 2023 het artikel is gepubliceerd. Deze Cochrane review includeerde drie RCT’s.
Twee RCT’s beschreven de vergelijking van 2% chloorhexidine in 70% isopropylalcohol (2% CHG in 70% IPA) met 10% povidonjodium (10% PI) voor de uitkomstmaat lijnsepsis. De risk ratio (RR) was 1.32 (95% CI: 0,53-3,25) op basis van de uitkomsten van één RCT (overlap definitie van lijnsepsis met mogelijke lijnsepsis), omdat in de andere studie géén lijnsepsis werd gerapporteerd. Dit is een klinisch relevant verschil, echter vanwege beperkingen in de studieopzet en imprecisie is de kwaliteit van het bewijs zeer laag.
In de RCT waarin géén lijnsepsis werd gerapporteerd, werd wel de uitkomstmaat mogelijke lijnsepsis beschreven. De RR was 1.00 (95% CI: 0,07-15,08). Dit is geen klinisch relevant verschil. De kwaliteit van deze studie werd beoordeeld als zeer laag door beperkingen in de studieopzet en imprecisie.
Beide RCT’s beschreven de uitkomstmaat chemische brandwonden (contactdermatitis). De ‘gepoolde’ RR was 1.04 (95% CI: 0,24-4,48). Dit is geen klinisch relevant verschil. De kwaliteit van deze studie werd beoordeeld als zeer laag door beperkingen in de studieopzet en imprecisie.
Eén RCT beschreef de vergelijking van 2% CHG in 70% IPA met 2% chloorhexidine in water (2% CHG-A). Deze studie rapporteerde voor de uitkomstmaten lijnsepsis een RR van 0.80 (95% CI: 0,34 -1,87) en voor mogelijke lijnsepsis een RR van 1.14 (95% CI: 0,34-3,84). Dit zijn geen klinisch relevante verschillen. De kwaliteit van deze studies werd beoordeeld als zeer laag door beperkingen in de studieopzet en imprecisie.
Voor de uitkomstmaat chemische brandwonden (contactdermatitis) werd een RR gerapporteerd van 0.98 (95% CI: 0,47-2,03). Dit is geen klinisch relevant verschil. De kwaliteit van deze studie werd beoordeeld als laag waarbij is afgewaardeerd voor imprecisie.
Op basis van de literatuur van (zeer) lage kwaliteit lijkt er een verlaagde kans te zijn op het optreden van lijnsepsis bij het gebruik van 2% chloorhexidine in 70% isopropylalcohol (2% CHG in 70% IPA) in vergelijking met het gebruik van 10% povidonjodium (10% PI). Er lijkt geen verschil te zijn in het optreden van lijnsepsis tussen het gebruik van 2% chloorhexidine in 70% isopropylalcohol (2% CHG in 70% IPA) en 2% chloorhexidine in water (2% CHG-A). Er lijkt ook geen verschil te zijn in het optreden van chemische brandwonden (contactdermatitis) tussen het gebruik 2% chloorhexidine in 70% isopropylalcohol (2% CHG in 70% IPA), 2% chloorhexidine in water (2%CHG-A) of 10% povidonjodium (10% PI).
Andere relevante uitkomsten uit de literatuur
In de geïncludeerde Cochrane-review werden, naast de uitkomstmaten zoals uitgewerkt in de literatuuranalyse, de volgende uitkomstmaten gerapporteerd voor huiddesinfectie voorafgaand aan het plaatsen van een centrale katheter bij neonaten:
-
Mogelijke sepsis
Garland (2009) constateerde dat er geen verschil was in het gebruik van 2% CHG in 70% IPA en 10% PI (RR=1,00; 95% BI: 0,28-3,54) op het vóórkomen van mogelijke sepsis. Kieran (2018) constateerde dat mogelijke sepsis kwam vaker voor bij gebruik van 2% CHG in 70% IPA (9,9%) dan bij gebruik van 10% PI (8,9%). Muhd Helmi (2023) berekende een ‘gepoolde’ RR van 1,11 (95% BI: 0,58-2,11).
-
Kolonisatie van de katheter
Garland (2009) constateerde dat kolonisatie van de katheter vaker voorkwam bij gebruik van 2% CHG in 70% IPA (12,5%) dan bij gebruik van 10% PI (4,2%). De RR was 3,00 (95%BI: 0,34-26,84). Clarke (2019) constateerde dat kolonisatie van de katheter minder vaak voorkwam bij gebruik van 2% CHG in 70% IPA (3,8%) dan bij gebruik van 2% CHG-A (7,4%). De RR was 0,51 (95% BI: 0,09-2,91).
-
Vroegtijdige verwijdering van de katheter
Clarke (2019) constateerde dat vroegtijdige verwijdering van de katheter vanwege een infectie minder vaak voorkwam bij gebruik van 2% CHG in 70% IPA (10,1%) dan bij gebruik 2% CHG-A (11,1%). De RR was 0,91 (95% BI: 0,26-3,19).
-
Sterfte door alle oorzaken/algemeen
Kieran (2018) constateerde dat ‘all-cause’ sterfte minder vaak voorkwam bij gebruik van 2% CHG in 70% IPA (10,1%) dan bij gebruik van 10% PI (11,5%). De RR was 0,88 (95% BI: 0,46-1,68).
-
Waarde thyroidstimulerend hormoon (TSH)
Kieran (2018) beschreef een verhoogde waarde van thyroidstimulerend hormoon (TSH) in neonaten bij gebruik van 10% PI in de screening (7,7%) en in serum (6,4%).
-
Chloorhexidineconcentratie in serum
De chloorhexidine concentratie in serum bij gebruik van 2% CHG in 70% IPA uit de studie van Garland (2009) was 13 tot 100 ng/mL. In de studie van Sharma (2021) werd geen verschil gezien in de plasmaconcentraties bij gebruik van chloorhexidine tussen de 1% CHG en 2% CHG.
Voor de uitkomstmaat toxiciteit kan op basis van de literatuur geen uitspraak gedaan worden welk middel een voorkeur heeft aangezien niet goed werd gedefinieerd wat toxische spiegels daadwerkelijk zijn.
De beschreven literatuur beschrijft het inbrengen van een centrale lijn. De werkgroep acht het onwaarschijnlijk dat de effectiviteit of bijwerkingen van een huiddesinfectiemiddel anders zijn bij het verrichten van een andere ingreep dan het inbrengen van een centrale lijn.
Chloorhexidine is in een oplossing verkrijgbaar in zowel water, als ethanol/isopropylalcohol. 0,5% chloorhexidine in alcohol opgelost betreft altijd ethanol, en een hoger percentage chloorhexidine (2%) in alcohol opgelost betreft isopropylalcohol (Chloraprep of Soluprep) (CBG/EMA).
In het geval van overgevoeligheid/allergie voor chloorhexidine kan voor een desinfectans gekozen worden op basis van jodium (bijvoorbeeld povidonjodium of jodiumtinctuur).
Waarden en voorkeuren van patiënten (en eventueel hun verzorgers)
Voor patiënten is het van belang dat iedere medische handeling veilig plaatsvindt, in dit geval het desinfecteren van de huid voorafgaand aan een ingreep bij prematuren dan wel neonaten. Verwacht wordt dat de ouders van deze patiëntenpopulatie geen voorkeur zullen hebben voor een huiddesinfectiemiddel, behalve wanneer sprake blijkt te zijn van een allergie of overgevoeligheidsreactie.
Kosten (middelenbeslag)
Kosten voor huiddesinfectiemiddelen zijn laag en zullen naar verwachting geen bepalende rol spelen in het al dan niet aanschaffen van hiervan.
Aanvaardbaarheid, haalbaarheid en implementatie
De werkgroep verwacht geen problemen in de aanvaardbaarheid, haalbaarheid en implementatie van de aanbeveling omdat deze aansluit bij de huidige praktijk.
Duurzaamheid
Bij het gebruik van huiddesinfectiemiddelen is het belangrijk dat organisaties middelen inkopen op basis van de behoefte van de instellingen en er geen te grote voorraad aangelegd wordt. Hiermee wordt voorkomen dat middelen weggegooid moeten worden omdat de expiratiedatum is verstreken. Daarnaast kunnen instellingen in hun aanschaf rekening houden met productie, transport, en gebruik van verpakkingsmateriaal.
Rationale van de aanbeveling
De werkgroep sluit zich aan bij de uitkomsten van de literatuur mede gezien de overeenkomst met de huidige praktijk waarbij in de meeste ziekenhuizen chloorhexidine opgelost in alcohol wordt gebruikt.
Onderbouwing
Autorisatiedatum: 29 augustus 2024
Eerstvolgende beoordeling actualiteit: 2026
Initiatief:
- Samenwerkingsverband Richtlijnen Infectiepreventie (SRI)
Geautoriseerd door:
- Nederlandse Vereniging voor Medische Microbiologie (NVMM)
- Nederlandse Vereniging voor Dermatologie en Venereologie (NVDV)
- Nederlandse Vereniging voor Heelkunde (NVvH)
- Nederlands Oogheelkundig Gezelschap (NOG)
- Nederlandse Orthopaedische Vereniging (NOV)
- Nederlandse Vereniging voor Reumatologie (NVR)
- Nederlandse Vereniging voor Thoraxchirurgie (NVT)
- Nederlandse Vereniging voor Kindergeneeskunde (NVK)
- Nederlandse Vereniging van Arbeidshygiëne (NVvA)
- Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg (VHIG)
- Patiëntenfederatie Nederland (PFNL)
Regiehouder:
- Samenwerkingsverband Richtlijnen Infectiepreventie
De ontwikkeling/herziening van deze richtlijnmodule is ondersteund door het Kennisinstituut van de Federatie Medisch Specialisten en is gefinancierd door het ministerie van VWS (Ministerie van Volksgezondheid, Welzijn en Sport). De financier heeft geen enkele invloed gehad op de inhoud van de richtlijnmodule.
Desinfectie van de huid/slijmvliezen in prematuren en neonaten is extreem belangrijk, omdat deze groep een verhoogd risico heeft op de ontwikkeling van zorggerelateerde infecties. Bekend is dat prematuren ernstige bijwerkingen, bijvoorbeeld brandwonden, kunnen krijgen van het (verkeerd) desinfecteren van de huid met chloorhexidine (-oplossingen). Chloorhexidine lijkt ondanks de bijwerkingen wel het meest gebruikte huiddesinfectiemiddel in deze patiëntenpopulatie. De vraag welk huiddesinfectiemiddel effectief en het meest veilig is in gebruik bij deze patiëntenpopulatie is tot op heden niet uitgebreid onderzocht.
A systematic review of the literature was performed to answer the following question:
Which skin antiseptic agent used prior to surgery is effective and safe to prevent infection in preterm or premature infants/neonates?
P: Preterm or premature infant/neonate.
I: Antiseptic skin preparation agents (chlorhexidine, povidone-iodine, octenidine, hexachlorophene, olanexidine, isopropyl alcohol) or concentrations in aqueous and alcohol-based solutions, sterile water.
C: Antiseptic skin preparation agents (chlorhexidine, povidone-iodine, octenidine, hexachlorophene, olanexidine, isopropyl alcohol) or concentrations in aqueous and alcohol-based solutions, sterile water.
O: Healthcare-associated infections (HAIs), adverse effects/reactions, toxicity.
Relevant outcome measures
The guideline development group considered healthcare-associated infection, adverse effects/reactions, toxicity as critical outcome measures for decision making.
A priori, the working group did not define the outcome measures listed above but used the definitions used in the studies.
The working group defined a 25% relative difference (RR < 0.8 or > 1.25) for dichotomous outcome infection as minimal clinically (patient) important difference.
Search and select (methods)
The databases Medline (via OVID), Embase (via embase.com), and Cinahl were searched with relevant search terms until 22 December 2022. The detailed search strategy is available on request (via info@sri-richtlijnen.nl). The systematic literature search resulted in 400 hits. Studies were selected based on the following criteria:
- Systematic review (SR; detailed search strategy, risk of bias assessment, and results of individual comparative studies available), randomised control trial or observational comparative study;
- Research question includes all elements of the PICO;
- Full tekst available;
- Full text written in English or Dutch.
Based on title and abstract screening, 29 studies were selected. From the selection, a study protocol was identified regarding antiseptic solutions for skin preparation during central catheter insertion in neonates from the Cochrane Database of Systematic Reviews. Information regarding the expected publication date was requested from the author, who indicated that it was scheduled for May 2023. After reading the full text, all other studies were excluded (see table of excluded studies).
Results
One systematic review was included. Important study characteristics and results are summarised in the evidence table. The assessment of the risk of bias is summarised in the risk of bias tables. The summary of literature, results, and evidence tables are included in Onderbouwing.
Description of studies
Muhd Helmi (2023) conducted a Cochrane systematic review (SR) to assess the safety and efficacy of different antiseptic skin preparation agents prior to central catheter placement in neonates. CENTRAL, MEDLINE, Embase, and trial registries were searched until 22 April 2022 without limitation of publication year. The review encompassed all (cluster)-RCTs that evaluated the efficacy of antiseptic skin preparation agents, regardless of language. These trials compared the use of any antiseptic agent, either as a single agent or in combination, against different concentrations of the same antiseptic agent, alternative antiseptic agents, placebo, or no agent used prior to central catheter placement in neonates admitted to the neonatal intensive care unit (NICU). Cross-over trials and quasi-RCTs were excluded. The authors included three multicentre RCTs in the SR that involved 466 premature babies in total who were born between 26 and 35 weeks of pregnancy and had a birthweight between 1000 g and 2000 g. These neonates were admitted at a level-III NICU, and each neonate had only one central catheter at any time, either an umbilical venous catheter (UVC) or a peripherally inserted central catheter (PICC). Two trials (Garland, 2009, 48 neonates; Kieran, 2018, 304 neonates) compared 2% chlorhexidine in 70% isopropyl alcohol (2% CHG in 70% IPA) against 10% povidone-iodine (10 % PI) and one trial (Clarke, 2019, 114 neonates) compared CHG-IPA against 2% chlorhexidine in aqueous solution (2% CHG-A). The outcomes reported in the review that met our outcomes of interest were catheter-related blood stream infection (CRBSI; infection originated from the central line), central line-associated bloodstream infection (CLABSI; infection possibly originated from the central line), and chemical burns.
Garland (2009) and Clarke (2019) used similar definition for CRBSI and CLABSI, whereas the definitions of CRBSI and CLABSI used by Kieran (2018) overlapped with each another. All studies were performed in high-income countries. The inclusion criteria employed by each trial differed from each another, however subgroup analyses were not feasible due to insufficient data. Each trial applied different antiseptic measures for catheter care, however sensitivity analyses was not applied due to the low number of included trials. Studies were assessed for methodological quality, including sequence generation, allocation concealment, blinding of participants and personnel, blinding of outcome assessment, incomplete outcome data, selective reporting, and any another bias, using the Cochrane ‘Risk of bias’ tool.
Results
1. Healthcare-associated infections
Catheter-related blood stream infection (CRBSI)
Comparison 2% CHG in 70% IPA versus 10% PI
Garland (2009) reported no events in either the intervention group or the control group. Kieran (2018) found that CRBSI occurred more often in the CHG-IPA group (6.8%) compared to the PI-group (5.1%) even though the definitions applied for CRBSI and CLABSI overlapped. The risk ratio (RR) was 1.32 (95%CI 0.53 to 3.25). This is a clinically relevant difference.
Comparison 2% CHG in 70% IPA versus 2% CHG-A
Clarke (2019) found that CRBSI occurred less often in the CHG-IPA group (17.7%) compared to the CHG-A group (22.2%). The RR was 0.80 (95% CI 0.34 to 1.87). This is not a clinically relevant difference.
Central line-associated bloodstream infection (CLABSI)
Comparison 2% CHG in 70% IPA versus 10% PI
In contrast to Kieran (2018, see CRBSI above), Garland (2009) used a separate definition of CLABSI. CLABSI occurred in both CHG-IPA and CHG-A group equally often (4.2%). The RR was 1.00 (95%CI 0.07 to 15.08) and thereby there is no difference in occurrence of CLABSI in using either CHG-IPA or PI.
Comparison 2% CHG in 70% IPA versus 2% CHG-A
Clarke (2019) found that CLABSI occurred more often in the CHG-IPA group (12.7%) compared to the CHG-A group (11.1%). The RR was 1.14 (95% CI 0.34 to 3.84). This is not a clinically relevant difference.
2. Adverse effects/reactions
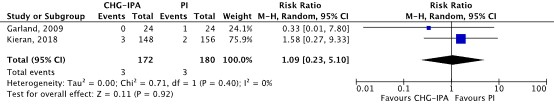
Chemical burns
Comparison 2% CHG in 70% IPA versus 10% PI
Garland (2009) and Kieran (2018) found that chemical burns occurred more often in the CHG-IPA group (1.7%) compared to the PI-group (1.7%). The pooled RR was 1.09 (95%CI 0.23 to 5.10; using random effects). This is not a clinically relevant difference. No heterogeneity was found (I2 = 0%).
Comparison 2% CHG in 70% IPA versus 2% CHG-A
Clarke (2019) found that chemical burns occurred less often in the CHG-IPA group (25.3%) compared to the CHG-A group (25.9%). The RR was 0.98 (95% CI 0.47 to 2.03). This is not a clinically relevant difference.
Level of evidence of the literature
In the included systematic review statistical significance was used as a threshold for clinically important difference. The working group defined a 25% relative difference (RR < 0.8 or > 1.25) for dichotomous outcome infection as minimal clinically (patient) important difference and therefore the GRADE (Grading Recommendations Assessment, Development and Evaluation ) conclusion in our summary is different then the GRADE conclusion in the systematic review.
1. Healthcare-associated infections
Catheter-related blood stream infection (CRBSI)
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
The level of evidence regarding the outcome measure CRBSI (with an overlap in definition with CLABSI) started at high and was downgraded by three levels to very low because of study limitations (-1; risk of bias: no blinding of participants and outcome assessors), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
The level of evidence regarding the outcome measure CRBSI started at high and was downgraded by three levels to very low because of study limitations (-1; risk of bias: missing data larger than difference between events in intervention and control group), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
Central line-associated bloodstream infection (CLABSI)
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
The level of evidence regarding the outcome measure CLABSI started at high and was downgraded by three levels to very low because of study limitations (-1; risk of bias: no blinding of participants and outcome assessors, selective reporting unclear), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
The level of evidence regarding the outcome measure CLABSI started at high and was downgraded by three levels to very low because of because of study limitations (-1; risk of bias: missing data larger than difference between events in intervention and control group), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
2. Adverse effects/reactions
Chemical burns
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
The level of evidence regarding the outcome measure chemical burns started at high and was downgraded by three levels to very low because of study limitations (-2; risk of bias: no blinding of participants and outcome assessors, selective reporting unclear), and imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
The level of evidence regarding the outcome measure chemical burns started at high and was downgraded by two levels to low because of imprecision (-2; confidence interval overlaps both threshold for minimal clinically important difference).
Healthcare-associated infections
1. Catheter-related bloodstream infection
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
|
Very low GRADE (Grading Recommendations Assessment, Development and Evaluation ) |
The evidence is very uncertain about the effect of 2% chlorhexidine in 70% isopropyl alcohol on catheter-related bloodstream infection, that in the included study overlaps in definition with a central line-associated bloodstream infection, when compared to 10% povidone iodine prior to central catheter placement in neonates. Source: Kieran, 2018 |
|---|
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
|
Very low GRADE |
The evidence is very uncertain about the effect of 2% chlorhexidine in 70% isopropyl alcohol on catheter-related bloodstream infection when compared to 2% chlorhexidine in aqueous solution prior to central catheter placement in neonates. Source: Clarke, 2019 |
|---|
2. Central line-associated bloodstream infection
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
|
Very low GRADE |
The evidence is very uncertain about the effect of 2% chlorhexidine in 70% isopropyl alcohol on central line-associated bloodstream infection when compared to 10% povidone iodine prior to central catheter placement in neonates. Source: Garland, 2009 |
|---|
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
|
Very low GRADE |
The evidence is very uncertain about the effect of 2% chlorhexidine in 70% isopropyl alcohol on central line-associated bloodstream infection when compared to 2% chlorhexidine in aqueous solution prior to central catheter placement in neonates. Source: Clarke, 2019 |
|---|
Adverse effects/reactions
Chemical burns
a. 2% chlorhexidine in 70% isopropyl alcohol versus 10% povidone iodine
|
Very low GRADE |
The evidence is very uncertain about the effect of 2% chlorhexidine in 70% isopropyl alcohol on chemical burns when compared to 10% povidone iodine prior to central catheter placement in neonates. Source: Garland, 2009; Kieran, 2018 |
|---|
b. 2% chlorhexidine in 70% isopropyl alcohol versus 2% chlorhexidine in aqueous solution
|
Low GRADE |
The evidence suggests that 2% chlorhexidine in 70% isopropyl alcohol results in little to no difference in chemical burns when compared with 2% chlorhexidine in aqueous solution prior to central catheter placement in neonates. Source: Clarke, 2019 |
|---|
Muhd Helmi MA, Lai NM, Van Rostenberghe H, Ayub I, Mading E. Antiseptic solutions for skin preparation during central catheter insertion in neonates. Cochrane Database Syst Rev. 2023 May 4;5(5):CD013841. Doi: 10.1002/14651858.CD013841.pub2. PMID: 37142550; PMCID: PMC10158577.
Bekijk de Evidence-tabel:
|
Reference |
Reason for exclusion |
|---|---|
|
Aitken J, Williams FL. A systematic review of thyroid dysfunction in preterm neonates exposed to topical iodine. Arch Dis Child Fetal Neonatal Ed. 2014 Jan;99(1):F21-8. doi: 10.1136/archdischild-2013-303799. Epub 2013 Oct 8. PMID: 24105624. |
Wrong sudy design, review did not fully meet criteria for a SR. Cochrane review with RCTs (Muhd Helmi, 2023) available |
|
Beekman K, Steward D. Chlorhexidine Gluconate Utilization for Infection Prevention in the NICU: A Survey of Current Practice. Adv Neonatal Care. 2020 Feb;20(1):38-47. doi: 10.1097/ANC.0000000000000658. PMID: 31567183. |
Survey of current practice |
|
Ness MJ, Davis DM, Carey WA. Neonatal skin care: a concise review. Int J Dermatol. 2013 Jan;52(1):14-22. doi: 10.1111/j.1365-4632.2012.05687.x. PMID: 23278604. |
Narrative review with recommendations |
|
Ng AL, Jackson C, Kazmierski M. Evaluation of Antiseptic Use in Pediatric Surgical Units in the United Kingdom-Where Is the Evidence Base? Eur J Pediatr Surg. 2016 Aug;26(4):309-15. doi: 10.1055/s-0035-1559883. Epub 2015 Sep 17. PMID: 26378485. |
Survey of current practice and narrative review |
|
Clarke P, Craig JV, Wain J, Tremlett C, Linsell L, Bowler U, Juszczak E, Heath PT. Safety and efficacy of 2% chlorhexidine gluconate aqueous versus 2% chlorhexidine gluconate in 70% isopropyl alcohol for skin disinfection prior to percutaneous central venous catheter insertion in preterm neonates: the ARCTIC randomised-controlled feasibility trial protocol. BMJ Open. 2019 Feb 19;9(2):e028022. doi: 10.1136/bmjopen-2018-028022. PMID: 30782955; PMCID: PMC6411256. |
This is protocol. Pre-results of this study were incorporated into the Cochrane review from Muhd Helmi included in the literature review of this module |
|
Garland JS, Alex CP, Mueller CD, Otten D, Shivpuri C, Harris MC, Naples M, Pellegrini J, Buck RK, McAuliffe TL, Goldmann DA, Maki DG. A randomized trial comparing povidone-iodine to a chlorhexidine gluconate-impregnated dressing for prevention of central venous catheter infections in neonates. Pediatrics. 2001 Jun;107(6):1431-6. doi: 10.1542/peds.107.6.1431. PMID: 11389271. |
Wrong comparison, 10% PI skin disinfection vs 70% alcohol skin disinfection by placement of chlorhexidine-impregnated dressing over insertion site |
|
Garland JS, Alex CP, Uhing MR, Peterside IE, Rentz A, Harris MC. Pilot trial to compare tolerance of chlorhexidine gluconate to povidone-iodine antisepsis for central venous catheter placement in neonates. J Perinatol. 2009 Dec;29(12):808-13. doi: 10.1038/jp.2009.161. Epub 2009 Oct 8. PMID: 19812587. |
Study included in Cochrane review Muhd Helmi |
|
Jain A, Deshpande P, Yoon EW, Lee KS, McGeer A, Shah V. 2% aqueous vs alcohol-based chlorhexidine for skin antisepsis in VLBW neonates undergoing peripheral venipuncture: a non-inferiority trial. J Perinatol. 2022 May;42(5):636-641. doi: 10.1038/s41372-022-01337-1. Epub 2022 Feb 19. PMID: 35184146. |
Published within period of search by Muhd Helmi (Cochrane review). Colony forming units is wrong outcome. Adverse skin reaction no events reported in both groups |
|
Kieran EA, O'Sullivan A, Miletin J, Twomey AR, Knowles SJ, O'Donnell CPF. 2% chlorhexidine-70% isopropyl alcohol versus 10% povidone-iodine for insertion site cleaning before central line insertion in preterm infants: a randomised trial. Arch Dis Child Fetal Neonatal Ed. 2018 Mar;103(2):F101-F106. doi: 10.1136/archdischild-2016-312193. Epub 2017 Oct 26. PMID: 29074717. |
Study included in Cochrane review Muhd Helmi |
|
Nuntnarumit P, Sangsuksawang N. A randomized controlled trial of 1% aqueous chlorhexidine gluconate compared with 10% povidone-iodine for topical antiseptic in neonates: effects on blood culture contamination rates. Infect Control Hosp Epidemiol. 2013 Apr;34(4):430-2. doi: 10.1086/669863. Epub 2013 Feb 14. PMID: 23466918. |
Wrong outcome, blood culture contamination |
|
Sathiyamurthy S, Banerjee J, Godambe SV. Antiseptic use in the neonatal intensive care unit - a dilemma in clinical practice: An evidence based review. World J Clin Pediatr. 2016 May 8;5(2):159-71. doi: 10.5409/wjcp.v5.i2.159. PMID: 27170926; PMCID: PMC4857229. |
Wrong study design, narrative review |
|
Sharma A, Kulkarni S, Thukral A, Sankar MJ, Agarwal R, Deorari AK, Mohapatra S, Velpandian T, Bajpai M. Aqueous chlorhexidine 1% versus 2% for neonatal skin antisepsis: a randomised non-inferiority trial. Arch Dis Child Fetal Neonatal Ed. 2021 Nov;106(6):643-648. doi: 10.1136/archdischild-2020-321174. Epub 2021 Jun 9. PMID: 34108192; PMCID: PMC8543223. |
Cochrane review with RCT available for outcome chemical burns (contact dermatitis). Colony forming units and plasma chlorhexidine levels were not outcomes of interest. |
|
Abdel-Sayed P, Tornay D, Hirt-Burri N, de Buys Roessingh A, Raffoul W, Applegate LA. Implications of chlorhexidine use in burn units for wound healing. Burns. 2020 Aug;46(5):1150-1156. doi: 10.1016/j.burns.2019.12.008. Epub 2020 Jan 3. PMID: 31911075. |
Chlorhexidine in burn care |
|
Lacaita MV, Cherchi S, Scalone L, Gadaleta A, Faggiano ME. Use and safety of antiseptics and disinfectants in pediatrics age. Giornale Italiano di Farmacia Clinica. 2020;34(3):129-144. |
Wrong language, Italian |
|
Lai NM, Taylor JE, Tan K, Choo YM, Ahmad Kamar A, Muhamad NA. Antimicrobial dressings for the prevention of catheter-related infections in newborn infants with central venous catheters. Cochrane Database Syst Rev. 2016 Mar 23;3(3):CD011082. doi: 10.1002/14651858.CD011082.pub2. PMID: 27007217; PMCID: PMC6464939. |
Wrong comparisons, different dressings (antiseptic- and antibiotic) |
|
Lund C, Kuller J, Lane A, Lott JW, Raines DA. Neonatal skin care: the scientific basis for practice. Neonatal Netw. 1999 Jun;18(4):15-27. doi: 10.1891/0730-0832.18.4.15. PMID: 10633681. |
Background information on neonatal skin |
|
Muhd Helmi!MA, Lai!NM, Van Rostenberghe!H, Ayub!I, Mading!E. |
This is protocol for a Cochrane review. The publication of this review is included. |
|
Sondhi V, Gupta G, Patnaik S. Preventing neonatal sepsis: Evidence-based approach for level 2 and 3 units. Journal of Neonatology. 2009 Jan-March;23(1),22-33. doi:10.1177/0973217920090105 |
Narrative review with recommendations |
|
Taylor JE, McDonald SJ, Tan K. Prevention of central venous catheter-related infection in the neonatal unit: a literature review. J Matern Fetal Neonatal Med. 2015 Jul;28(10):1224-30. doi: 10.3109/14767058.2014.949663. Epub 2014 Sep 26. PMID: 25076387. |
Narrative review |
|
Cobett S, LeBlanc A. IV site infection: a prospective, randomized clinical trial comparing the efficacy of three methods of skin antisepsis. Candaian Intravenous Nurses Association. 1999;15(0):48-49 |
Full tekst not available |
|
Curry S, Honeycutt M, Goins G, Gilliam C. Catheter-associated bloodstream infections in the NICU: getting to zero. Neonatal Netw. 2009 May-Jun;28(3):151-5. doi: 10.1891/0730-0832.28.3.151. PMID: 19451076. |
Introducing new intervention to bundle (CHG skin antisepsis and CHG patch around catheter insertion site) |
|
Pettit JD, Sharpe EL. The Effect of Education on Chlorhexidine Use in the NICU. Neonatal Netw. 2017 Sep 1;36(5):294-305. doi: 10.1891/0730-0832.36.5.294. PMID: 28847353. |
Wrong study, survey on knowledge and attitudes regarding use and removal of CHG antiseptic |
|
Dutta S, Logan S, Gilbert R. Impact of newborn skin-cleansing with chlorhexidine on neonatal mortality in southern Nepal. Pediatrics. 2007 Sep;120(3):693-4; author reply 694-5. doi: 10.1542/peds.2007-1042. PMID: 17766550. |
Wrong study design, comment |
|
Jokar A, Mohebi Z, Garmaznejad S, Sharifi M. A Comparison of Efficacy of Isopropyl Alcohol and Ethanol in Disinfection Programs in Pediatrics Ward and Neonatal Intensive Care Unit. Journal of Hayat 2009; 15 (3) :52-58 |
Wrong language, Iranian |
|
Oishi T, Iwata S, Nonoyama M, Tsuji A, Sunakawa K. Double-blind comparative study on the care of the neonatal umbilical cord using 80% ethanol with or without chlorhexidine. J Hosp Infect. 2004 Sep;58(1):34-7. doi: 10.1016/j.jhin.2004.03.027. PMID: 15350711. |
Wrong outcome, colonisation by Staphylococcus aureus |
|
Pezzati M, Rossi S, Tronchin M, Dani C, Filippi L, Rubaltelli FF. Umbilical cord care in premature infants: the effect of two different cord-care regimens (salicylic sugar powder vs chlorhexidine) on cord separation time and another outcomes. Pediatrics. 2003 Oct;112(4):e275. doi: 10.1542/peds.112.4.e275. PMID: 14523211. |
Wrong comparison, salicylic sugar powder vs chlorhexidine |
|
Taylor JE, McDonald SJ, Tan K. A survey of central venous catheter practices in Australian and New Zealand tertiary neonatal units. Aust Crit Care. 2014 Feb;27(1):36-42. doi: 10.1016/j.aucc.2013.11.002. Epub 2013 Dec 4. PMID: 24315154. |
Survey of current practice |
|
Shah D, Tracy M. Cutaneous antisepsis for prevention of intravascular catheter–associated infection in newborn infants. Cochrane Database Syst Rev. 2020 Apr 21;2020(4):CD011043. doi: 10.1002/14651858.CD011043.pub2. PMCID: PMC7173700. |
Withdrawal from publication due to insufficient progress |
|
Cucurachi G, Tuoto MG. I disinfettanti per la cute del prematuro [Disinfectants for the skin of premature]. Minerva Pediatr. 2010 Jun;62(3 Suppl 1):157-9. Italian. PMID: 21090087. |
Wrong language, Italian |
Bijlagen
|
Begrip |
Definitie |
|---|---|
|
Algemene voorzorgsmaatregelen |
Maatregelen die bij elke patiënt ongeacht zijn/haar infectiestatus of kolonisatie van toepassing zijn. Deze maatregelen staan beschreven in de SRI (Samenwerkingsverband Richtlijnen Infectiepreventie )-richtlijnen Handhygiëne & persoonlijke hygiëne medewerker, Persoonlijke beschermingsmiddelen, Reiniging & desinfectie van ruimten en Accidenteel bloedcontact. |
|
Infectie |
Interactie tussen het micro-organisme en de gastheer leidt tot schade of een veranderde fysiologie bij de gastheer. De schade of veranderde fysiologie kan resulteren in klinisch waarneembare symptomen en verschijnselen maar ook langdurig onopgemerkt blijven of subklinisch verlopen. |
|
Rondom het oog |
Hiermee wordt perioculair bedoeld. |
|
Transmissie |
Overdracht van micro-organismen. |
|
Wondclassificaties |
Ingrepen worden aan de hand van de wondclassificatie (CDC) ingedeeld in de volgende categorieën, die correleren met het risico op postoperatieve wondinfecties: 1) schoon 2) schoon-besmet 3) besmet en 4) vuil). Een schone wond valt daarom onder categorie 1. Een niet-schone wond valt onder categorie 2, 3 of 4.
|
Werkwijze
AGREE
Deze richtlijnmodule is opgesteld volgens de eisen vermeld in het rapport Medisch Specialistische Richtlijnen 2.0 van de adviescommissie Richtlijnen van de Raad Kwaliteit. Dit rapport is gebaseerd op het AGREE II instrument (Appraisal of Guidelines for Research & Evaluation II; Brouwers, 2010).
Knelpuntenanalyse en uitgangsvragen
Tijdens de voorbereidende fase inventariseerde de werkgroep de knelpunten in de zorg voor patiënten waarbij de huid wordt gedesinfecteerd voorafgaand aan een ingreep, punctie/biopsie en injectie. De werkgroep beoordeelde de aanbeveling(en) uit de eerdere WIP-richtlijnen Desinfectie huid en slijmvliezen en Puncties op noodzaak tot revisie. Tevens zijn er knelpunten aangedragen door IGJ, KNMP (Koninklijke Nederlandse Maatschappij ter bevordering der Pharmacie ), NAPA (Nederlandse Associatie Physician Assistants ), NOG (Nederlands Oogheelkundig Gezelschap ), NVAB (Nederlandse Vereniging voor Arbeids- en Bedrijfsgeneeskunde ), NVALT (Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose ), NVvC, NVDV (Nederlandse Vereniging voor Dermatologie en Venereologie ), NVIC, NVK (Nederlandse Vereniging voor Kindergeneeskunde ), NVKC, NVKF (Nederlandse Vereniging voor Klinische Fysica ), NVKG, NVMM (Nederlandse Vereniging voor Medische Microbiologie ), NVPC, NVU, NVvA (Nederlandse Vereniging voor Arbeidshygiëne ), NVR, NVvR (Nederlandse Vereniging voor Radiologie ), NVZ, NVZA (Nederlandse Vereniging van Ziekenhuisapothekers ), SNV, VCCN, VDSMH (Vereniging Deskundigen Steriele Medische Hulpmiddelen ), Verenso (Vereniging van specialisten ouderengeneeskunde ) en VHIG (Vereniging voor Hygiëne & Infectiepreventie in de Gezondheidszorg ) via een schriftelijke knelpunteninventarisatie. Een verslag hiervan is opgenomen onder aanverwante producten.
Op basis van de uitkomsten van de knelpuntenanalyse zijn door de werkgroep concept-uitgangsvragen opgesteld en definitief vastgesteld.
Uitkomstmaten
Na het opstellen van de zoekvraag behorende bij de uitgangsvraag inventariseerde de werkgroep welke uitkomstmaten voor de patiënt relevant zijn, waarbij zowel naar gewenste als ongewenste effecten werd gekeken. Hierbij werd een maximum van acht uitkomstmaten gehanteerd. De werkgroep waardeerde deze uitkomstmaten volgens hun relatieve belang bij de besluitvorming rondom aanbevelingen, als cruciaal (kritiek voor de besluitvorming), belangrijk (maar niet cruciaal) en onbelangrijk. Ook definieerde de werkgroep tenminste voor de cruciale uitkomstmaten welke verschillen zij klinisch (patiënt) relevant vonden.
Methode literatuursamenvatting
Een uitgebreide beschrijving van de strategie voor zoeken en selecteren van literatuur is te vinden onder Zoeken en selecteren onder Onderbouwing. Indien mogelijk werd de data uit verschillende studies gepoold in een random-effects model. Review Manager 5.4 werd gebruikt voor de statistische analyses. De beoordeling van de kracht van het wetenschappelijke bewijs wordt hieronder toegelicht.
Beoordelen van de kracht van het wetenschappelijke bewijs
De kracht van het wetenschappelijke bewijs werd bepaald volgens de GRADE-methode. GRADE staat voor Grading Recommendations Assessment, Development and Evaluation (zie www.gradeworkinggroup.org). De basisprincipes van de GRADE-methodiek zijn: het benoemen en prioriteren van de klinisch (patiënt) relevante uitkomstmaten, een systematische review per uitkomstmaat, en een beoordeling van de bewijskracht per uitkomstmaat op basis van de acht GRADE-domeinen (domeinen voor downgraden: risk of bias, inconsistentie, indirectheid, imprecisie, en publicatiebias; domeinen voor upgraden: dosis-effect relatie, groot effect, en residuele plausibele confounding).
GRADE onderscheidt vier gradaties voor de kwaliteit van het wetenschappelijk bewijs: hoog, redelijk, laag en zeer laag. Deze gradaties verwijzen naar de mate van zekerheid die er bestaat over de literatuurconclusie, in het bijzonder de mate van zekerheid dat de literatuurconclusie de aanbeveling adequaat ondersteunt (Schünemann, 2013; Hultcrantz, 2017).
|
GRADE |
Definitie |
|---|---|
|
Hoog |
|
|
Redelijk |
|
|
Laag |
|
|
Zeer laag |
|
Bij het beoordelen (graderen) van de kracht van het wetenschappelijk bewijs in richtlijnen volgens de GRADE-methodiek spelen grenzen voor klinische besluitvorming een belangrijke rol (Hultcrantz, 2017). Dit zijn de grenzen die bij overschrijding aanleiding zouden geven tot een aanpassing van de aanbeveling. Om de grenzen voor klinische besluitvorming te bepalen moeten alle relevante uitkomstmaten en overwegingen worden meegewogen. De grenzen voor klinische besluitvorming zijn daarmee niet een-op-een vergelijkbaar met het minimaal klinisch relevant verschil (minimal clinically important difference (MCID)). Met name in situaties waarin een interventie geen belangrijke nadelen heeft en de kosten relatief laag zijn, kan de grens voor klinische besluitvorming over de effectiviteit van de interventie bij een lagere waarde (dichter bij het nuleffect) liggen dan de MCID (Minimal Clinically Important Difference ) (Hultcrantz, 2017).
Overwegingen (van bewijs naar aanbeveling)
Om te komen tot een aanbeveling zijn naast (de kwaliteit van) het wetenschappelijke bewijs ook andere aspecten belangrijk en worden meegewogen, zoals aanvullende argumenten uit bijvoorbeeld de biomechanica of fysiologie, waarden en voorkeuren van patiënten, kosten (middelenbeslag), aanvaardbaarheid, haalbaarheid en implementatie. Deze aspecten zijn systematisch vermeld en beoordeeld (gewogen) onder het kopje Overwegingen en kunnen (mede) gebaseerd zijn op expert opinion. Hierbij is gebruik gemaakt van een gestructureerd format gebaseerd op het evidence-to-decision-framework van de internationale GRADE Working Group (Alonso-Coello, 2016a; Alonso-Coello 2016b). Dit evidence-to-decision-framework is een integraal onderdeel van de GRADE-methodiek.
Formuleren van aanbevelingen
De aanbevelingen geven antwoord op de uitgangsvraag en zijn gebaseerd op het beschikbare wetenschappelijke bewijs en de belangrijkste overwegingen, en een weging van de gunstige en ongunstige effecten van de relevante interventies. De kracht van het wetenschappelijk bewijs en het gewicht dat door de werkgroep wordt toegekend aan de overwegingen, bepalen samen de sterkte van de aanbeveling. Volgens de GRADE-methodiek sluit een lage bewijskracht van conclusies in de systematische literatuuranalyse een sterke aanbeveling niet a priori uit, en zijn bij een hoge bewijskracht ook zwakke aanbevelingen mogelijk (Agoritsas, 2017; Neumann, 2016). De sterkte van de aanbeveling wordt altijd bepaald door weging van alle relevante argumenten tezamen. De werkgroep heeft bij elke aanbeveling opgenomen hoe zij tot de richting en sterkte van de aanbeveling zijn gekomen.
In de GRADE-methodiek wordt onderscheid gemaakt tussen sterke en zwakke (of conditionele) aanbevelingen. De sterkte van een aanbeveling verwijst naar de mate van zekerheid dat de voordelen van de interventie opwegen tegen de nadelen (of vice versa), gezien over het hele spectrum van patiënten waarvoor de aanbeveling is bedoeld. De sterkte van een aanbeveling heeft duidelijke implicaties voor patiënten, behandelaars en beleidsmakers (zie onderstaande tabel). Een aanbeveling is geen dictaat, zelfs een sterke aanbeveling gebaseerd op bewijs van hoge kwaliteit (GRADE-gradering HOOG) zal niet altijd van toepassing zijn, onder alle mogelijke omstandigheden en voor elke individuele patiënt.
Implicaties van sterke en zwakke aanbevelingen voor verschillende richtlijngebruikers
|
|
Sterke aanbeveling |
Zwakke (conditionele) aanbeveling |
|---|---|---|
|
Voor patiënten |
De meeste patiënten zouden de aanbevolen interventie of aanpak kiezen en slechts een klein aantal niet. |
Een aanzienlijk deel van de patiënten zouden de aanbevolen interventie of aanpak kiezen, maar veel patiënten ook niet. |
|
Voor behandelaars |
De meeste patiënten zouden de aanbevolen interventie of aanpak moeten ontvangen. |
Er zijn meerdere geschikte interventies of aanpakken. De patiënt moet worden ondersteund bij de keuze voor de interventie of aanpak die het beste aansluit bij zijn of haar waarden en voorkeuren. |
|
Voor beleidsmakers |
De aanbevolen interventie of aanpak kan worden gezien als standaardbeleid. |
Beleidsbepaling vereist uitvoerige discussie met betrokkenheid van veel stakeholders. Er is een grotere kans op lokale beleidsverschillen. |
Organisatie van zorg
In de knelpuntenanalyse en bij de ontwikkeling van de richtlijnmodule is expliciet aandacht geweest voor de organisatie van zorg: alle aspecten die randvoorwaardelijk zijn voor het verlenen van zorg (zoals coördinatie, communicatie, (financiële) middelen, menskracht en infrastructuur). Randvoorwaarden die relevant zijn voor het beantwoorden van deze specifieke uitgangsvraag zijn genoemd bij de overwegingen.
Commentaar- en autorisatiefase
De conceptrichtlijnmodule werd aan de betrokken (wetenschappelijke) verenigingen en (patiënten) organisaties voorgelegd ter commentaar. De commentaren werden verzameld en besproken met de werkgroep. Naar aanleiding van de commentaren werd de conceptrichtlijnmodule aangepast en definitief vastgesteld door de werkgroep. De definitieve richtlijnmodule werd aan de deelnemende (wetenschappelijke) verenigingen en (patiënt) organisaties voorgelegd voor autorisatie en door hen geautoriseerd dan wel geaccordeerd.
Inbreng patiëntenperspectief
Er werd aandacht besteed aan het patiëntenperspectief door uitnodigen van Patiëntfederatie Nederland (PFNL) voor de schriftelijke knelpuntenanalyse. De verkregen input is meegenomen bij het opstellen van de uitgangsvragen, de keuze voor de uitkomstmaten en bij het opstellen van de overwegingen. De conceptrichtlijn is ook voor commentaar voorgelegd aan PFNL (Patiëntfederatie Nederland ) en de eventueel aangeleverde commentaren zijn bekeken en verwerkt.
Wkkgz (Wet kwaliteit, klachten en geschillen zorg ) & Kwalitatieve raming van mogelijke substantiële financiële gevolgen
Bij de richtlijn is in overeenstemming met de Wet kwaliteit, klachten en geschillen zorg (Wkkgz) een kwalitatieve raming uitgevoerd of de aanbevelingen mogelijk leiden tot substantiële financiële gevolgen. Bij het uitvoeren van deze beoordeling zijn richtlijnmodules op verschillende domeinen getoetst (zie het stroomschema op de Richtlijnendatabase).
Uit de kwalitatieve raming blijkt dat er waarschijnlijk geen substantiële financiële gevolgen zijn, zie onderstaande tabel.
|
Module |
Uitkomst raming |
Toelichting |
|---|---|---|
|
Module 1. Huiddesinfectie |
||
|
Module 1.1. Ingrepen algemeen |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft]. Er worden daarom geen financiële gevolgen verwacht. |
|
Module 1.2 Bloedafname en injecties |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft]. Er worden daarom geen financiële gevolgen verwacht. |
|
Module 1.3 Hoofd-halsgebied en oog |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het overgrote deel (± 90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
|
Module 1.4 Prematuren/neonaten |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het overgrote deel (± 90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
|
Module 2. Algemene voorzorgsmaatregelen |
||
|
Module 2.1 Punctie/biopsie/injectie buiten het OK-complex |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het geen nieuwe manier van zorgverlening of andere organisatie van zorgverlening betreft, het geen toename in het aantal in te zetten voltijdsequivalenten aan zorgverleners betreft en het geen wijziging in het opleidingsniveau van zorgpersoneel betreft]. Er worden daarom geen financiële gevolgen verwacht. |
|
Module 2.2 Intra-articulaire injectie/punctie |
Geen financiële gevolgen |
Hoewel uit de toetsing volgt dat de aanbeveling(en) breed toepasbaar zijn (> 40.000 patiënten), volgt uit de toetsing dat het overgrote deel (± 90%) van de zorgaanbieders en zorgverleners al aan de norm voldoet. Er worden daarom geen financiële gevolgen verwacht. |
Literatuur
Agoritsas T, Merglen A, Heen AF, Kristiansen A, Neumann I, Brito JP, Brignardello-Petersen R, Alexander PE, Rind DM, Vandvik PO, Guyatt GH. UpToDate adherence to GRADE criteria for strong recommendations: an analytical survey. BMJ Open. 2017 Nov 16;7(11):e018593. doi: 10.1136/bmjopen-2017-018593. PubMed PMID: 29150475; PubMed Central PMCID: PMC5701989.
Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Rada G, Rosenbaum S, Morelli A, Guyatt GH, Oxman AD; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 1: Introduction. BMJ. 2016 Jun 28;353:i2016. doi: 10.1136/bmj.i2016. PubMed PMID: 27353417.
Alonso-Coello P, Oxman AD, Moberg J, Brignardello-Petersen R, Akl EA, Davoli M, Treweek S, Mustafa RA, Vandvik PO, Meerpohl J, Guyatt GH, Schünemann HJ; GRADE Working Group. GRADE Evidence to Decision (EtD) frameworks: a systematic and transparent approach to making well informed healthcare choices. 2: Clinical practice guidelines. BMJ. 2016 Jun 30;353:i2089. doi: 10.1136/bmj.i2089. PubMed PMID: 27365494.
Brouwers MC, Kho ME, Browman GP, Burgers JS, Cluzeau F, Feder G, Fervers B, Graham ID, Grimshaw J, Hanna SE, Littlejohns P, Makarski J, Zitzelsberger L; AGREE Next Steps Consortium. AGREE II: advancing guideline development, reporting and evaluation in healthcare. CMAJ. 2010 Dec 14;182(18):E839-42. doi: 10.1503/cmaj.090449. Epub 2010 Jul 5. Review. PubMed PMID: 20603348; PubMed Central PMCID: PMC3001530.
Hultcrantz M, Rind D, Akl EA, Treweek S, Mustafa RA, Iorio A, Alper BS, Meerpohl JJ, Murad MH, Ansari MT, Katikireddi SV, Östlund P, Tranæus S, Christensen R, Gartlehner G, Brozek J, Izcovich A, Schünemann H, Guyatt G. The GRADE Working Group clarifies the construct of certainty of evidence. J Clin Epidemiol. 2017 Jul;87:4-13. doi: 10.1016/j.jclinepi.2017.05.006. Epub 2017 May 18. PubMed PMID: 28529184; PubMed Central PMCID: PMC6542664.
Medisch Specialistische Richtlijnen 2.0 (2012). Adviescommissie Richtlijnen van de Raad Kwaliteit.
Neumann I, Santesso N, Akl EA, Rind DM, Vandvik PO, Alonso-Coello P, Agoritsas T, Mustafa RA, Alexander PE, Schünemann H, Guyatt GH. A guide for health professionals to interpret and use recommendations in guidelines developed with the GRADE approach. J Clin Epidemiol. 2016 Apr;72:45-55. doi: 10.1016/j.jclinepi.2015.11.017. Epub 2016 Jan 6. Review. PubMed PMID: 26772609.
Schünemann H, Brożek J, Guyatt G, et al. GRADE handbook for grading quality of evidence and strength of recommendations. Updated October 2013. The GRADE Working Group, 2013.
Inleiding
Dit implementatieplan is opgesteld om de implementatie van de aanbevelingen in de richtlijn infectiepreventie Desinfectie huid en slijmvliezen plus puncties te borgen. Voor het opstellen van dit plan heeft de werkgroep per ontwikkelde module beoordeeld wat eventueel bevorderende en belemmerende factoren zijn voor het naleven van de aanbevelingen en wat eventueel nodig is om de aanbevolen infectiepreventiemaatregelen in Nederland te implementeren.
Werkwijze
De werkgroep heeft per aanbeveling binnen de modules geïnventariseerd:
- wat een realistische termijn voor implementatie is;
- de verwachtte effect van implementatie op de zorgkosten;
- randvoorwaarden om de aanbeveling tijdig te implementeren;
- mogelijk barrières voor implementatie;
- te ondernemen acties voor (bevordering van) implementatie;
- verantwoordelijke partij voor de te ondernemen acties.
Hieronder is een tabel (Tabel 1) opgenomen met alle modules uit deze richtlijn met daarbij de bijhorende implementatietermijn, verwacht effect op kosten, mogelijke barrières voor implementatie, te ondernemen acties voor implementatie en verantwoordelijken voor de acties.
Tabel 1. Implementatieplan
|
Module |
Tijdspad voor implementatie |
Verwacht effect op de kosten |
Mogelijke barrières voor implementatie |
Te ondernemen acties voor implementatie |
Verantwoordelijke voor acties
|
|---|---|---|---|---|---|
|
Noodzaak huid- en slijmvliesdesinfectie ingrepen |
< 1 jaar |
Kosten zullen ongeveer gelijk blijven |
Door voor ingrepen buiten de operatiekamer andere concentraties van het aanbevolen middel mee te nemen als er sprake is van onvoldoende beschikbaarheid van het middel, worden geen barrières voor implementatie verwacht. |
Verspreiden richtlijn en voorlichting zorgmedewerkers |
Professionals |
|
Huiddesinfectiemiddel hoofd-/hals en oog |
< 1 jaar |
Kosten zullen ongeveer gelijk blijven |
Geen, sluit aan bij huidige praktijk |
Verspreiden richtlijn en voorlichting zorgmedewerkers |
Professionals |
|
Huiddesinfectie bloedafname ja/nee |
< 1 jaar |
De kosten voor instellingen die voorheen geen huiddesinfectie toepasten zullen toenemen, echter er is geen sprake van een substantiële toename van kosten in z’n totaliteit. |
Mogelijk weerstand tegen een verandering in werkwijze |
Verspreiden richtlijn en voorlichting medewerkers |
Professionals |
|
Huiddesinfectie injectie ja/nee
|
< 1 jaar |
De kosten voor instellingen die voorheen wel huiddesinfectie toepasten zullen afnemen, echter er is geen sprake van een substantiële afname van kosten in z’n totaliteit. |
Mogelijk weerstand tegen een verandering in werkwijze |
Verspreiden richtlijn en voorlichting medewerkers |
Professionals |
|
Huiddesinfectiemiddel bloedafname en injectie
|
< 1 jaar |
Kosten zullen mogelijk minder worden door minder vaak bij injecties huiddesinfectie toe te passen. |
Geen, sluit aan bij huidige praktijk |
Verspreiden richtlijn en voorlichting medewerkers |
Professionals |
|
Huiddesinfectie prematuren/neonaten |
< 1 jaar |
Kosten zullen nagenoeg gelijk blijven. |
Geen, sluit aan bij huidige praktijk |
Verspreiden richtlijn en voorlichting zorgmedewerkers |
Professionals |
|
Algemene voorzorgsmaatregelen punctie |
< 1 jaar |
Kosten zullen nagenoeg gelijk blijven. |
Geen, sluit aan bij huidige praktijk |
Verspreiden richtlijn en voorlichting zorgmedewerkers |
Professionals |
|
Intra-articulaire injectie |
< 1 jaar |
Kosten zullen nagenoeg gelijk blijven. |
Geen, sluit aan bij huidige praktijk |
Verspreiden richtlijn en voorlichting zorgmedewerkers |
Professionals |
Termijn voor implementatie
Omdat de aanbevelingen in het algemeen nauw aansluiten bij de huidige klinische praktijk, voorziet de werkgroep nauwelijks belemmeringen voor implementatie. Als men ervan uitgaat dat alle betrokken zorgprofessionals vanaf autorisatie van deze richtlijn (voorzien begin 2024) binnen een jaar op de hoogte gesteld worden van deze richtlijn, is implementatie van de aanbevelingen vanaf een jaar later (begin 2025) realistisch en haalbaar.
Te ondernemen acties per partij
Hieronder wordt per partij toegelicht welke acties zij kunnen ondernemen om de implementatie van de richtlijn te bevorderen.
Alle direct betrokken wetenschappelijke verenigingen/beroepsorganisaties
- Bekend maken van de richtlijn onder de leden.
- Publiciteit voor de richtlijn door er over te vertellen op congressen.
- Ontwikkelen van gerichte bijscholing/trainingen om kennisoverdracht tussen medewerkers te faciliteren/stimuleren.
- Ontwikkelen en aanpassen van infectiepreventieprotocollen.
De lokale vakgroepen/individuele medisch professionals
- Het bespreken van de aanbevelingen in de multidisciplinaire teamoverleggen, vakgroepoverleggen en relevante lokale werkgroepen.
- Aanpassen lokale infectiepreventieprotocollen.
- Afstemmen en afspraken maken met andere betrokken disciplines om de toepassing van de aanbevelingen in de praktijk te borgen.
Samenwerkingsverband Richtlijnen Infectiepreventie (SRI):
- Toevoegen van de richtlijn aan de SRI (Samenwerkingsverband Richtlijnen Infectiepreventie )-website.
- Toevoegen van richtlijn aan richtlijnendatabase.
- Het implementatieplan wordt in de bijlage opgenomen, zodat deze voor op een voor alle partijen goed te vinden is.
- De kennislacunes worden opgenomen in de bijlagen.
Indicatoren
Voor deze richtlijn zijn geen indicatoren ontwikkeld.
Tijdens de ontwikkeling van de richtlijn Desinfectie huid en slijmvliezen plus puncties is systematisch gezocht naar onderzoeksbevindingen die nuttig konden zijn voor het beantwoorden van de uitgangsvragen. Een deel (of een onderdeel) van de hiervoor opgestelde zoekvragen is met het resultaat van deze zoekacties te beantwoorden, een deel echter niet. Door gebruik te maken van de evidence-based methodiek (EBRO) is duidelijk geworden dat er nog kennislacunes bestaan. De werkgroep is van mening dat (vervolg)onderzoek wenselijk is om in de toekomst een duidelijker antwoord te kunnen geven op vragen uit de praktijk. Om deze reden heeft de werkgroep per module aangegeven waar wetenschappelijke kennis beperkt is en dus op welke vlakken nader onderzoek gewenst is.
Module 1 Huiddesinfectie
Module 1.1 Huiddesinfectie ingrepen algemeen
Geen systematische search uitgevoerd.
Module 1.2 Bloedafname en injectie
Het is onduidelijk wat de plaats is van huiddesinfectie voorafgaand aan bloedafname ten behoeve van diagnostiek en keuringen op het voorkómen van een (lokale/systemische) infectie bij de patiënt?
Het is onduidelijk wat de plaats is van huiddesinfectie voorafgaand aan een intramusculaire, subcutane of intradermale injectie op het voorkómen van een infectie bij de patiënt?
Het is onduidelijk welk huiddesinfectiemiddel de voorkeur heeft om voorafgaand aan een bloedafname en/of een injectie (intramusculair, subcutaan, intradermaal) te gebruiken, om een infectie bij de patiënt te voorkómen en in geval van bloedafname het risico op contaminatie van het bloedmonster te reduceren? Echter de werkgroep is van mening dat de praktijk hierdoor niet gehinderd wordt en voert deze daarom niet als kennislacune op.
Module 1.3 Hoofd-halsgebied en oog
Er is onvoldoende bewijs over de optimale concentratie van povidonjodium voor desinfectie van het oogoppervlak.
Module 1.4 Prematuren/neonaten
Tot op heden is de vraag welk huiddesinfectiemiddel effectief en het meest veilig is in gebruik bij prematuren en neonaten niet uitgebreid onderzocht.
Module 2. Algemene voorzorgsmaatregelen Punctie/biopsie/injectie
Module 2.1 Punctie/biopsie/injectie
Bij nieuwe ontwikkelingen/interventies in de gezondheidszorg, waaronder puncties, zal op basis van best practices een keuze gemaakt worden over de te treffen infectiepreventiemaatregelen in overleg met de behandelaar. De werkgroep is van mening dat (vervolg)onderzoek wenselijk is om in de toekomst een duidelijker antwoord te kunnen geven op de noodzaak voor welke maatregelen uit het oogpunt van infectiepreventie nodig zijn en in het kader van de Greendeal niet onnodig getroffen worden.
Module 2.2 Intra-articulaire injectie
Wat is het effect van infectiepreventiemaatregelen op het ontstaan van zorggerelateerde infecties na een intra-articulaire injectie of punctie?
Overig/toekomstige knelpunten
Er is tot nu toe onvoldoende bekend over de aspecten voor duurzaamheid in relatie tot de voorkeur voor een bepaald desinfectiemiddel.
Bekijk de pdf met het overzicht van de ontvangen reacties voor een schriftelijke knelpuntenanalyse voor deze richtlijn.